宫颈癌疫苗快速过审具有示范意义
2018-05-07 粤港澳大湾区城市群网YGA.CN
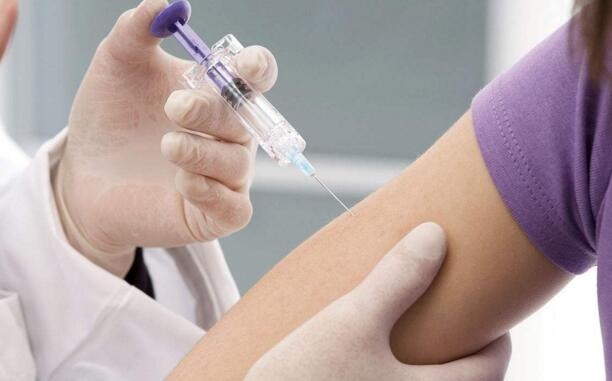
4月24日,国家药监局药品审评中心官网公示了第28批拟纳入优先审评程序名单,默沙东的9价HPV疫苗上市申请位列其中。公示信息显示,疫苗因符合“具有明显临床优势”的标准而被列入。4月29日晚间,国家药监局官方网站发布消息称,有条件批准用于预防宫颈癌的9价HPV疫苗上市,批准时间是4月28日。这距离4月20日国家药监局药审中心受理默沙东公司提交的9价HPV疫苗上市申请,仅仅过了8天。
2015年8月,国务院下发《关于改革药品医疗器械审评审批制度的意见》,拉开了中国药审制度改革大幕;2016年,药审改革配套措施之一的“优先审评”制度正式落地,临床急需药品将被优先审评审批;2017年,中共中央办公厅、国务院办公厅正式印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,“接受境外临床试验数据”的政策出台;同年12月,食药监总局发布《临床急需药品有条件批准上市的技术指南(征求意见稿)》,其中规定,用于治疗严重危及生命且尚无有效治疗手段的疾病的创新药,可基于特定情况而批准上市。9价HPV疫苗审批速度之快史无前例,被业内称为“火箭速度”,可以说受益于背后药审制度的深化改革。9价HPV疫苗的过审不是特例,而是第一个受益者。
自2006年全球第一支HPV疫苗上市至今已有10多年,从最早的2价、4价疫苗发展至目前全世界临床应用最为普遍的9价疫苗,让宫颈癌这种严重威胁全球女性生命健康的癌症可通过接种疫苗实现有效防范,这不得不说是一大福音。但由于此前我国药品审批制度的相对滞后,让这一医学成果迟迟未能为国内广大女性所享受。2016年7月有关部门批准2价HPV疫苗在中国内地上市时,4价疫苗早于几个月之前在美国停售——美国的疾病控制预防中心开始采购更为先进的9价HPV疫苗。同时,不少人不惜山长水远、费时费力地跑去香港接种9价HPV疫苗,甚至导致香港疫苗供货紧张,大幅推高疫苗价格,这些情况也进一步说明,国人对于优质医药医疗服务有着迫切需求。
此前我国药监部门并不认可新药在境外取得的临床试验数据,进口药必须在国内完成三期临床试验后才能获批上市。且不论临床需求是否迫切,新药上市前都要遵循先来后到,排队等待药监部门审批,加之药监部门审评人员短缺,导致药品审批通道常年堵塞。多种因素叠加,往往导致一种新药在欧美国家上市5到7年之后才能进入中国。这一问题影响的不仅是HPV疫苗的进口,很多时候一些治疗重症疾病的进口药由于迟迟无法在国内落地,导致患者不能及时使用特效药而延误治疗。
所以9价HPV疫苗的过审上市,其意义不仅在于降低广大女性的患病风险。对于一部分急需进口药物治病的患者而言,也意味着更高效的用药治疗。进口药审批问题可以说获得了相关部门的有效反馈,几年之间各项政策不断落地,从根本上构建起了药品进口审批的新机制,HPV疫苗的快速获批可以说极好地检验了这套新机制的有效性。9价疫苗快速获批的经验,对于其他药品加速进口是一次极好的示范。

 民生 医疗
民生 医疗